Los Ganglios o Nodos Linfáticos son pequeños órganos aplanados y de forma reniforme que se disponen en cadenas a lo largo del trayecto de los vasos linfáticos, su tamaño es muy variado dependiendo fundamentalmente de su grado de actividad. (1)
Son órganos encapsulados constituidos por tejido linfoide y que aparecen esparcidos por el cuerpo, siempre en el trayecto de los vasos linfáticos. Son de tamaño variable, miden entre 1 mm los más pequeños y entre 1-2 cm los de mayor tamaño, y se los encuentran en la axila, ingle, a lo largo de los grandes vasos del cuello y, en gran cantidad, en el tórax y en el abdomen, especialmente en el mesenterio. (5)
Su parénquima se compone de acumulaciones de Linfocitos T y B, células presentadoras de Antígenos y Macrófagos. Estas células linfoides reaccionan a la presencia de Antígenos mediante una respuesta inmunitaria en la que los Macrófagos fagocitan bacterias y otros microorganismos que entran al Ganglio Linfático a través de la linfa. (2)
Cada ganglio es una estructura blanda, que tiene una cápsula de tejido conectivo, por lo general rodeada de tejido adiposo. Posee un polo convexo perforado por vasos linfáticos aferentes, mientras que el polo opuesto, denominado hilio del Ganglio Linfático, que adopta una forma más o menos cóncava, es el sitio por el que las arterias y venas entran y salen del Ganglio. Además, la linfa sale del ganglio a través de vasos linfáticos eferentes que también se localizan en el hilio. (2)
Organización histológica(1,2)
Desde el punto de vista histológico, un Ganglio Linfático está formado por una masa de tejido linfoide envuelta por una cápsula de tejido conectivo. Está subdividido en una región Externa, denominada Corteza (intensamente teñida), y otra zona más Interna, la Médula (de tinción más pálida). Esta diferencia de tinción se debe a las diferencias en el número, diámetro y disposición de los senos linfáticos y también a la concentración algo mayor de Linfocitos en la Corteza. (1) Todas estas regiones tienen un abastecimiento abundante de sinusoides, espacios crecidos recubiertos por endotelio a través de los cuales se filtra la linfa. (2)
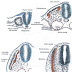
Desde la superficie interna de la cápsula se extienden trabéculas ramificadas de tejido conjuntivo denso hacia la profundidad del tejido linfoide. (1) La linfa ingresa por el lado convexo y sale por el lado cóncavo, donde está localizado el hilio del órgano. La sangre entra y sale por el hilio (ver fig. 01)
Fig. 01: Representación esquemática de la circulación de la sangre y la linfa en un Ganglio Linfático. El área más oscura, central, representa a medula del ganglio. En verde claro, la zona de flujo de la linfa: los senos linfáticos.
Fuente: Junqueira Carneiro J., Histología Básica
Cápsula(1,2)
Un Ganglio Linfático está rodeado de una cápsula de tejido conectivo de colágeno denso irregular, (2) que en su superficie externa se continúa con el tejido conectivo circundante. En uno de los bordes se distingue una hendidura, el hilio, donde la cápsula es más gruesa. Numerosas vías linfáticas aferentes atraviesan la cápsula en distintos sitios de la superficie convexa, mientras que escasas vías linfáticas eferentes abandonan el Ganglio Linfático por el hilio, donde además penetran los vasos sanguíneos al órgano. Desde la superficie interna de la cápsula se extienden cantidades variables de trabéculas ramificadas de tejido conectivo denso hacia el interior del tejido linfoide. (3) Estas trabéculas son bien desarrolladas en los Ganglios Linfáticos grandes, mientras que en los ganglios pequeños son delgadas e interrumpidas. Están poco desarrolladas en el abdomen. (1)

Fig. 02. Fotografía en la cual se aprecian tanto la cápsula de un Ganglio Linfático como su seno subcapsular. Fuente: Laboratorio FACISA-UNE.
Corteza(1)
Es una masa densa de células linfoides atravesadas por trabéculas y senos intermedios. Puede o no rodear por completo al Ganglio. Aquí se vuelven a diferenciar dos zonas: la Corteza externa y la interna. (1)
En cuanto a los cúmulos de tejido linfoide, podemos agruparlos en tres grupos diferentes:
1) Tejido linfoide difuso: abundante en la Corteza profunda. Aquí son muy numerosos los Linfocitos T.
2) Tejido linfoide primario: son zonas esféricas de Linfocitos pequeños empaquetados. Abundan los Linfocitos B. Pasan a convertirse en secundarios cuando van a producir más Linfocitos.
3) Tejido linfoide secundario: en el cual volvemos a distinguir dos zonas:
a) Centro germinal: es la parte central. Es lugar de diferenciación celular y producción de anticuerpos (abundantes Linfocitos B, y algunos Linfocitos T), formada por Linfocitos grandes y Macrófagos. De tinción pálida debido al abundante citoplasma y a los núcleos eucromáticos de las células.
b) Manto (zona creciente): formada por Linfocitos pequeños (tienen poco citoplasma, por eso es más oscura). Envuelve como un casquete o manto y está orientado hacia el lado de la cápsula.
Fig. 03. Corteza de un Ganglio Linfático. Fuente: Laboratorio FACISA-UNE
En cuanto a la distribución de los distintos tipos de Linfocitos, los Linfocitos B se concentran en mayor cantidad dentro de los centros germinales, y por ende, en la Corteza superficial. En oposición, los Linfocitos T se concentran en mayor cantidad en el tejido linfoide difuso de la Corteza profunda.
Como ya se ha mencionado antes, la Corteza profunda está subdividida en dos zonas: externa e interna.
1) Corteza externa: es aquí en donde se encuentran los tejidos linfoides primarios y secundarios.
2) Corteza interna [Corteza internodular o profunda]: aquí solo existe tejido linfoide difuso.
Es el único lugar donde es posible encontrar Linfocitos recirculantes y vénulas poscapilares con células altamente endoteliales (epitelio cúbico simple). Por estas vénulas pasan esos Linfocitos recirculantes. Las células altamente endoteliales poseen forma cuboidea baja, carecen de capa muscular y permiten el paso de los Linfocitos recirculantes.
Estos Linfocitos presentan en su membrana un receptor glucoproteico involucrado en el reconocimiento de las células altamente endoteliales.
Los Linfocitos aquí encontrados se disponen de forma más laxa que en la Corteza externa, y son de preferencia Linfocitos pequeños. Tanto los Linfocitos grandes, Macrófagos y células plasmáticas aquí son solo ocasionales.
Aquí también se encuentran las denominadas células interdigitadas, con un núcleo eucromático, citoplasma pálido, y abundantes prolongaciones que se interdigitan con los Linfocitos vecinos. Pueden presentar gránulos semejantes a los gránulos de Birbeck de las células de Langerhans. Manifiestan en su superficie moléculas del CMH II.
No existe límite de demarcación neto entre la Corteza externa y Corteza interna; la Corteza interna se continúa directamente con los cordones medulares.
Fig. 05. Sección histológica a poco aumento de um gânglio linfático completo.
Fuente: Finn Geneser - Atlas color de histología
Sistema de senos(1,3)
1) Vasos aferentes: llegan al Ganglio por su cara convexa, presentan válvulas que se abren (miran) hacia el ganglio. dentro de la cápsula sigue siendo aferente. Una vez atravesada la cápsula, forman el seno subcapsular.
2) Seno subcapsular [marginal] (de margen, por debajo de la cápsula): aquí ya no es un vaso redondeado, sino sólo una “cavidad” en forma de cuenco (plato). Se comunica con el linfático eferente a nivel de hilio. Esta cavidad está atravesada por pequeñas fibras colágenas.
Aquí pueden encontrarse células veladas, estas presentan pliegues ondulados y gránulos semejantes a las cel. Langerhans. Manifiestan en su superficie moléculas del CMH II.
3) Senos intermedios [corticales, o paratrabeculares]: es continuación del seno subcapsular. Siguen a las trabéculas. Son permeables, se hallan dentro del parénquima, terminan formando los senos medulares.
4) Senos medulares: ya dentro de la Médula. Comunican con el seno marginal a nivel del hilio. Son anchos, tortuosos, irregulares, ramificados y anastomosados. Son permeables para la linfa y elementos celulares. Los espacios entre ellos forman los cordones medulares.
5) Cordones medulares: son los espacios que quedan entre los senos medulares. Es una agregación de tejido linfoide. Aquí todavía pueden encontrarse trabéculas. Se anastomosan unos con otros terminando a nivel del hilio. Hay abundancia de Macrófagos, Linfocitos B, células y fibras reticulares, y determinados granulocitos.
6) Vasos eferentes: abandonan al ganglio por su cara cóncava, presentan válvulas que se orientan dándole la espalda al hilio.
El endotelio de los senos marginal e intermedio se tiñe fuertemente con plata, mientas que el endotelio del seno medular no lo hace.
La disposición que adoptan las válvulas de los vasos aferentes y eferentes mantiene el flujo unidireccional de la linfa, impidiendo el retroceso de ésta. (1)
Médula (1)
En los linfáticos abdominales aparece muy bien desarrollada (porque ahí están los Macrófagos y todo eso para fagocitar a los Antígenos del intestino). Los senos medulares están formados por células endoteliales planas. En su existe una red de células reticulares estrelladas. Están unidas a la pared y entre ellas. En su luz también encontramos Macrófagos. Estos Macrófagos son redondeados y están recubiertos por microvellosidades y procesos ondulantes. Son muy abundantes en los senos medulares.
Fig. 04. Cortes histológicos a nivel de la médula de dos Ganglios Linfáticos. Fuente: Laboratorio FACISA – UNE.
Vascularización (1,3)
Las arterias ingresan por el hilio y emiten ramificaciones arteriolares que transcurren por las trabéculas. Pronto las abandonan y pasan a los cordones medulares, que son irrigados por capilares. Algunas de las arteriolas continúan por los cordones hasta la Corteza, donde forman una red capilar, y luego corren vénulas poscapilares de regreso a través de la Corteza profunda hasta los cordones medulares, donde se unen para formar vénulas algo más grandes, que acompañan a las ramificaciones arteriolares hacia el exterior del Ganglio Linfático.
Las vénulas poscapilares de la Corteza profunda poseen un endotelio cúbico a cilíndrico, por lo que son vénulas de endotelio alto (3) (vénulas poscapilares altamente endoteliales) (1) (HEV). Como se mencionó al principio, los pequeños Linfocitos pasan de la sangre al parénquima del Ganglio Linfático a través de la pared de estas vénulas poscapilares de endotelio alto. Son Linfocitos T y B (no comprometidos, pero posiblemente también algunos Linfocitos memoria); los Linfocitos T permanecen en la Corteza profunda, mientras que los Linfocitos B migran a los folículos primarios de la Corteza externa. Durante su permanencia en el Ganglio Linfático los Linfocitos se fijan (mediante moléculas de adhesión celular) a las células presentadoras de Antígeno que se encuentran en su camino, dado que buscan en ellos el Antígeno extraño que el Linfocito es capaz de reconocer y para así activarse. Los Linfocitos B buscan los Antígenos unidos a la superficie de las células dendríticas foliculares, porque los Linfocitos B no requieren de la presentación del Antígeno para reaccionar con él. Si el Linfocito encuentra su Antígeno específico permanece en el Ganglio Linfático, puesto que se inicia una respuesta inmunológica. Por el contrario, si los Linfocitos no encuentran su Antígeno específico (lo que ocurre para la gran mayoría de los Linfocitos recirculantes, dado que solo uno de cada 108 de los Linfocitos es específico para un Antígeno determinado), tanto los Linfocitos T como los B abandonan el Ganglio Linfático por las vías linfáticas eferentes después de un periodo de unas 12 horas. Se desconoce el mecanismo por el cual los Linfocitos se localizan en las dos zonas mencionadas, pero es posible que tengan importancia los distintos tipos de células dendríticas. También puede desempeñar un papel la diferencia de los tipos de moléculas de adhesión sobre la superficie de los Linfocitos T y B. (3)

Fig. 05. Venas poscapilares altamente endoteliales. A. a La izquierda vista en um corte transversal. B. A La derecha um corte longitudinal. Fuente: Laboratorio FACISA – UNE.
Inervación. (1)
Penetran por el hilio junto con los vasos formando plexos perivasculares. En las trabéculas son fibras independientes, y luego en la corteza todos son vasomotores.(1)
Histofisiología. (3)
1) Filtración y fagocitosis.
Los Ganglios Linfáticos ejercen una acción filtrante sobre la linfa que los atraviesa. La linfa fluye a escasa velocidad a través de los senos y los filamentos reticulares que los cruzan actúan como filtro mecánico, que detiene o disminuye la velocidad de paso de microorganismos infecciosos y otras células. De este modo, éstos son presa fácil para la fagocitosis por los Macrófagos. Mediante la filtración, los Ganglios Linfáticos pueden retener más del 90% de los Antígenos que ingresan por las vías linfáticas aferentes. La linfa suele atravesar por lo menos dos Ganglios Linfáticos en su camino desde los tejidos hacia la sangre. De este modo, en condiciones normales, los Ganglios Linfáticos eliminan bacterias ya partículas de tamaño equivalente que se encuentran en la linfa circulante. En consecuencia, ante una infección aguda se produce una rápida dilatación de los senos de los Ganglios Linfáticos de drenaje, con ingreso de granulocitos neutrófilos desde los vasos sanguíneos, en especial de la Médula. Estas células fagocitan con gran efectividad las bacterias de la linfa e incrementan en muy alto grado la capacidad de los Ganglios Linfáticos para impedir la diseminación de la infección al torrente sanguíneo. Si la infección no se combate con rapidez, aumenta notablemente la cantidad de Macrófagos en el Ganglio Linfático.
Los Ganglios Linfáticos sólo retienen parte de las células cancerosas transportadas por la linfa. Si estas células pasan al sistema linfático pueden difundir al organismo por el torrente sanguíneo, proceso denominado metástasis.
La acción filtrante de los Ganglios Linfáticos en enfermedades infecciosas y malignas a menudo causa aumento de su tamaño incluso de sensibilidad. En consecuencia, la búsqueda de Ganglios Linfáticos aumentados de tamaño y dolorosos es un importante eslabón en el diagnóstico clínico y, especialmente en las enfermedades malignas, tiene gran valor al evaluar el pronóstico.
2) Funciones inmunológicas.
Si la linfa que ingresa por las vías linfáticas aferentes al Ganglio Linfático contiene un Antígeno extraño (ya sea libre o unido a células presentadoras de Antígeno) que aparece por primera vez en el organismo, se produce una respuesta inmunológica primaria en el Ganglio Linfático. El Antígeno es retenido en el ganglio al ser captado y presentado por células dendríticas interdigitantes y Macrófagos, y por fijación a la superficie de las células dendríticas foliculares; debido al encuentro con los Linfocitos no comprometidos recirculantes con receptores específicos para el Antígeno, los Linfocitos no comprometidos se activan y se inicia la respuesta inmunológica. Esta respuesta siempre se inicia con la activación de Linfocitos Th no comprometidos de la Corteza profunda (la zona dependiente del timo), que unas 48 horas después de la activación aumentan de tamaño y se desarrollan a linfoblastos que sufren varias divisiones. Así, después de cinco días se observa gran cantidad de linfoblastos en la Corteza profunda, que entonces se diferencian a Linfocitos Th efectores y memoria, por lo que también se encuentra gran cantidad de pequeños Linfocitos en la Corteza profunda. Si el Antígeno extraño es intracelular, lo cual ocurre con frecuencia, por ejemplo con virus, también se infectan las células dendríticas, que presentan el virus relacionado con moléculas del CMH clase I y así inician la activación de los Linfocitos Tc. Con la ayuda de los Linfocitos Th (de tipo TH1), se activan por completo los Linfocitos Tc y se transforman en linfoblastos proliferantes. Las células formadas se diferencian en Linfocitos citotóxicos efectores (CTL) y Linfocitos Tc memoria, que representan parte de la cantidad incrementada de pequeños Linfocitos en la Corteza profunda. Las células efectoras formadas abandonan en gran número el Ganglio Linfático y, dado que la diferenciación modifica la expresión de las moléculas de adhesión, las células se ubican en las zonas inflamadas donde comienzan a combatir el Antígeno.
Al mismo tiempo que ocurre esta parte celular de la respuesta inmunológica en el Ganglio Linfático, casi siempre también tienen lugar rápidamente después de la activación de los Linfocitos Th una activación de los Linfocitos B no comprometidos, con el consiguiente inicio de una respuesta inmunológica humoral. La primera fase de esta respuesta también comienza en la Corteza profunda, dado que Linfocitos B no comprometidos allí ubicados, con receptores específicos para el Antígeno en cuestión reaccionan con él (cabe recordar que los Linfocitos B pueden reconocer el Antígeno solo, sin su presentación unida a una molécula de CMH). Los Linfocitos B no comprometidos son reclutados por migración desde los folículos primarios en la Corteza hacia la Corteza profunda o por pasaje a través de la pared de las vénulas poscapilares de endotelio alto. Después de unirse al Antígeno, los Linfocitos B no comprometidos lo captan por endocitosis mediada por receptor y lo presentan a los Linfocitos Th activados (te tipo Th2) o a Linfocitos Th no comprometidos que así se activan por presentación del Antígeno. En ambos casos, el conjugado de Linfocitos T y B con contacto físico entre ´si conduce a la activación del Linfocito B como consecuencia de la función auxiliar del Linfocito Th, por lo que el Linfocito B se diferencia a linfoblasto y sufre proliferación durante los siguientes 4-5 días. De este modo se generan pequeños focos en la Corteza profunda, y las células plasmáticas que allí se forman secretan anticuerpos (IgM e IgG) que llegan al torrente sanguíneo con la linfa eferente. Durante la respuesta inmunológica primaria la mayor parte del anticuerpo formado por las células plasmáticas proviene de estos focos. Gradualmente tiene lugar la migración de las células plasmáticas hacia la Médula, donde se ubican en los cordones medulares.
Pocos días después de la formación de los pequeños focos en la Corteza profunda, una pequeña cantidad de los Linfocitos B y Th activados abandona los pequeños focos primarios y migra a los folículos primarios de la Corteza externa. Tras la activación total de los Linfocitos B, con formación de un conjugado con los Linfocitos Th, los Linfocitos B se transforman en linfoblastos, que comienzan a sufrir muy activa proliferación en la porción central del folículo primario. Estos linfoblastos también se denominan centroblastos, y su proliferación causa proliferación de un centro germinativo en el folículo, que así se transforma en un folículo secundario. En este proceso, los Linfocitos T originales, no activados (no específicos para el Antígeno en cuestión), son empujados hacia la periferia del folículo, donde conforman la condensación periférica que incluye a la calota. Los centroblastos en proceso de proliferación se desplazan en forma gradual hacia una mitad del centro germinativo, donde generan la zona oscura, mientras que gran número de pequeños Linfocitos originados como sucesores de las células en proceso de proliferación, y denominados centrocitos, migran hacia la mitad contraria del centro germinativo, donde, junto con numerosas células dendríticas foliculares allí presentes, forman la zona clara.
Durante la proliferación, los centroblastos sufren hipermutación somática con maduración por afinidad, por lo que los centrocitos generados adquieren diferente afinidad por el Antígeno ingresante (si bien todos son específicos para ese Antígeno, también tienen distinta capacidad de unión). A continuación, en la zona clara tiene lugar una selección, dado que los centrocitos reaccionan con el Antígeno unido a la superficie de las células dendríticas, y todos los centrocitos sin capacidad de unirse al Antígeno o con baja afinidad por él son descartados y sufren muerte por apoptosis, para después ser fagocitados por los Macrófagos. Sólo una cantidad menor de los centrocitos con elevada afinidad por el Antígeno son seleccionados para proseguir la diferenciación, con formación de Linfocitos B memoria y plasmablastos. Algunos Linfocitos B memoria permanecen en el folículo y pasan a formar parte de la condensación periférica que incluye la calota, pero el resto abandona el Ganglio Linfático por las vías linfáticas eferentes y recirculan. Los plasmablastos migran hacia la Médula, donde se diferencian en células plasmáticas y se ubican en los cordones medulares.
Una vez seleccionados los centrocitos con elevada afinidad para su diferenciación, pueden sufrir variación de clase, por lo que la cadena pesada varía de un isotipo a otro, mientras que la porción variable permanece sin modificaciones, es decir, no se modifica la especificidad por el Antígeno. Por ejemplo, de este modo una molécula de IgM se puede transformar en una molécula de IgG con la misma especificidad. La variación de clase depende del medio en que tiene lugar la proliferación, y así las células plasmáticas originadas en los ganglios intestinales casi todas producirán IgA, mientras que las células plasmáticas generadas, por ejemplo, en el bazo, casi exclusivamente producen IgG.
Es típico que los centros germinativos comiencen a aparecer alrededor de una semana después de la exposición al Antígeno, y experimentos han demostrado que todos los Linfocitos B de cada centro germinativo se originan a partir de una única célula o de unos pocos Linfocitos B activados, y todos son específicos para el mismo Antígeno.
Una vez interrumpido el estímulo antigénico, por ejemplo por eliminación de la infección, involucionan los centros germinativos y los Linfocitos B parecen sufrir muerte celular programada.
Durante la respuesta inmunológica se observa un notable incremento de la Corteza profunda, al mismo tiempo que se forman los centros germinativos, por lo que aumentan de tamaño los folículos y, en consecuencia, todo el Ganglio Linfático. El grado de modificación de las Cortezas profunda y externa depende del tipo de estimulación antigénica y la reacción es más notable en la Corteza profunda en una respuesta inmunológica a predominio celular (donde dominan los Linfocitos T en proceso de proliferación), por ejemplo debido a un trasplante de piel genéticamente incompatible.
El aumento de tamaño del Ganglio Linfático también se debe a que la estimulación antigénica incrementa la intensidad de la recirculación, por lo que es mayor la cantidad de Linfocitos que atraviesan el Ganglio Linfático desde el torrente sanguíneo, con mayor probabilidad de que lo encuentren los Linfocitos no comprometidos específicos para el Antígeno. Así, durante la respuesta inmunológica, en la linfa eferente se detectan anticuerpos secretados por las células plasmáticas generadas en el Ganglio Linfático y también se observa gran cantidad de Linfocitos, como consecuencia de la mayor circulación y de la formación de nuevos Linfocitos por los procesos proliferativos durante la respuesta inmunológica.
Ante una respuesta inmunológica secundaria por un nuevo ingreso al organismo del mismo Antígeno extraño que desencadenó la reacción inmunológica primaria, se observan los mismos procesos antes descritos, pero mucho más rápidos y más intensos. Como se vio antes, esto se debe a que existe un gran clon de Linfocitos T y B memoria específicos para el Antígeno en cuestión y a que es más fácil activar los Linfocitos memoria. No obstante, es muy importante que ya existan anticuerpos circulantes con elevada afinidad por el Antígeno, por lo que grandes cantidades de complejo Antígeno-anticuerpo llegan hasta los Ganglios Linfáticos regionales con la linfa aferente. Allí se unen con la superficie de las prolongaciones de las células dendríticas foliculares donde son retenidos durante periodos prolongados, hasta años. En consecuencia, tienen lugar una activación notable de los Linfocitos B, por lo que las células dendríticas foliculares, cuyas prolongaciones presentan engrosamientos como cadenas de perlas, liberan las “perlas” como estructuras limitadas por membrana densamente cubiertas por complejos de Antígeno-anticuerpo en la superficie. Estas estructuras, denominadas iccosomas son captadas por los Linfocitos B por endocitosis mediada por receptores después de la unión del Antígeno, ubicado sobre la superficie del iccosoma, con los receptores de superficie del Linfocito B. Además, es característico de la respuesta inmunológica secundaria (y una posible terciaria, y las posteriores) que la mayor parte de la gran cantidad de plasmablastos que ahora se forman abandonen el Ganglio Linfático y se ubiquen en la Médula ósea, donde se diferencian en células plasmáticas secretoras de anticuerpo. Así se demostró que hasta el 90% de las moléculas de anticuerpo producidas por inmunizaciones repetidas provienen de estas células plasmáticas en la Médula ósea. (3)
Bibliografía
1) Bloom, Fawcett, W. / Tratado de Histología / 12ª edición / Editorial Mc Graw – Hill Interamericana / Año 1996/ España / Madrid.
2) Gartner, L. – Hiatt, J. / Texto - Atlas de Histología / 3ª edición /Editorial Mc Graw Hill Interamericana / Año 2008/ México.
3) Geneser, Finn - Histología / 3ª edición / Editorial Médica Panamericana / Año 2000 / España / Madrid.
4) Geneser, Finn - Atlas color de histología / 3ª edición / Editorial Médica Panamericana/ Año 2000 / España / Madrid..
5) Junqueira, L. C. – Carneiro J., Histología Básica / 10ª edición / Editorial Guanabara Koogan S.A / Año 2004 / Rio de Janeiro / Brasil.